Scienziati trovano l’interruttore per la crescita dei vasi sanguigni
Notch
Alcuni ricercatori europei hanno identificato un interruttore che stimola o inibisce la crescita dei vasi sanguigni. Le scoperte, pubblicate sulla rivista Cell, potrebbero contribuire allo sviluppo di trattamenti per malattie e disturbi caratterizzati da una crescita eccessiva o insufficiente dei vasi sanguigni.
Durante lo sviluppo, la crescita e la guarigione, nuovi vasi sanguigni formano una rete intricata – moltiplicandosi dove è necessario – per assicurare che tutti i tessuti ricevano un flusso costante di ossigeno e sostanze nutritive. Quando durante questo processo qualcosa va storto, i risultati possono essere disastrosi; gli infarti infatti accadono quando si blocca l’afflusso di sangue al cuore. In questo caso, gli scienziati vorrebbero sapere come stimolare la crescita di nuovi vasi sanguigni nel cuore. D’altra parte, i tumori cancerosi sono tenuti in vita da una rete di vasi sanguigni, in questo caso bloccando la crescita di nuovi vasi sanguigni si potrebbe efficacemente debilitare il tumore.
Gli scienziati hanno a lungo cercato il meccanismo che determina quando un vaso sanguigno si ramifica in due e quando non lo fa. In questo recente studio, scienziati tedeschi e britannici hanno identificato un interruttore molecolare che controlla il destino di singole cellule.
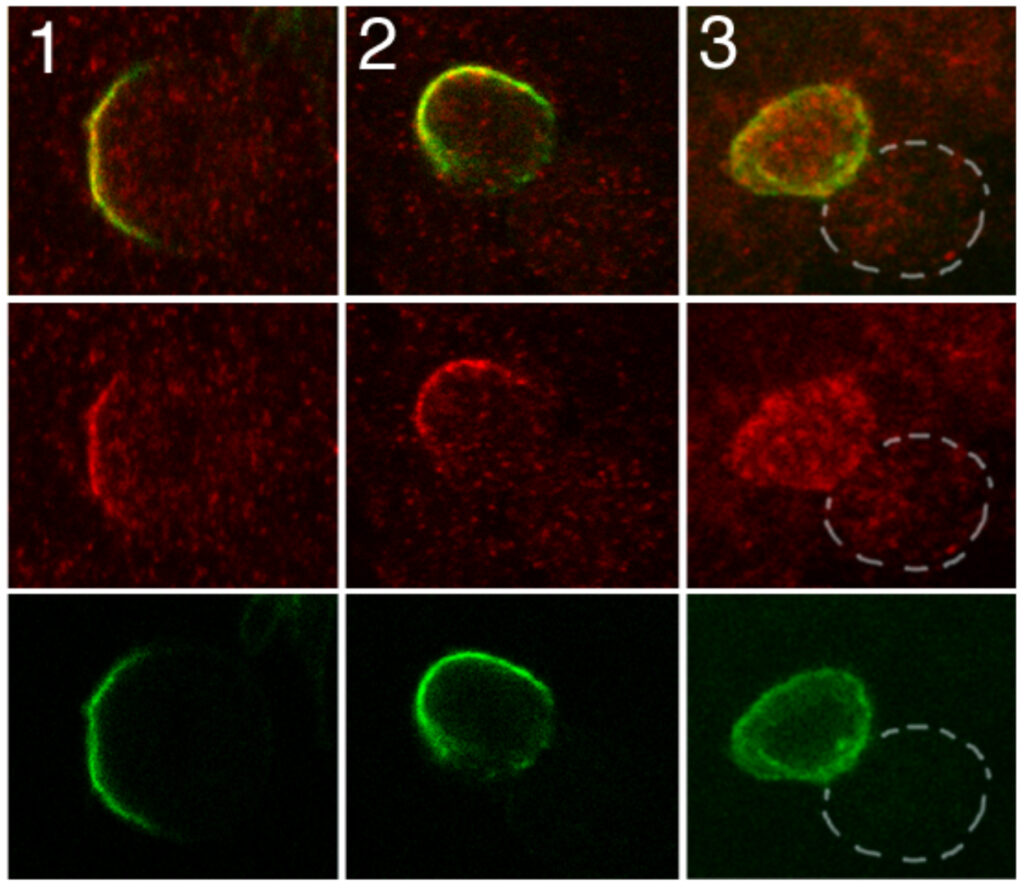
L’interruttore in questione coinvolge una proteina chiamata Notch, che si trova sulla superficie delle cellule che ricoprono le pareti del vaso sanguigno. Diverse proteine possono attaccarsi alla Notch, alcune la attivano e altre la disattivano.
Se la Notch è attivata, la cellula diventa sensibile ad una molecola chiamata Fattore di crescita endoteliale vascolare (VEGF). Come suggerisce il nome stesso, il VEGF stimola la crescita di nuovi vasi sanguigni. In questo studio i ricercatori hanno scoperto che una proteina chiamata “Jagged1” attiva la Notch e quindi provoca la formazione di nuovi vasi sanguigni. La Jagged1 sta sulla superficie delle cellule ed è quindi in grado di attaccarsi agli interruttori Notch di cellule vicine.
“Per la prima volta riusciamo a capire come questi componenti individuali funzionano insieme,” ha commentato il professor Ralf Adams dell’Istituto Max Planck di biomedicina molecolare in Germania. “Vogliamo scoprire – tramite esperimenti su topi – come controllare attivamente la crescita di vasi sanguigni.” Un giorno si potrebbero usare medicine per fare lo stesso nelle persone, ha aggiunto.
Attualmente alcuni tipi di cancro e di malattie degli occhi si curano bloccando l’attività del VEGF. Queste cure sono però costose e gli effetti collaterali le rendono inadatte a molti pazienti. “Chiarendo la funzione della Jagged1, speriamo di aver trovato una vera alternativa per terapie future,” ha detto il dott. Rui Benedito, anch’egli dell’Istituto Max Planck di biomedicina molecolare.
Il passo successivo per i ricercatori consiste nello studiare in modo esauriente l’efficacia dei trattamenti che interferiscono con la Notch e se essi comportino effetti collaterali pericolosi. È una questione importante perché la Notch ha importanti funzioni, per esempio nello sviluppo del sistema nervoso e immunitario.
“Notch, Dll4 [una proteina che rallenta la formazione di nuovi vasi sanguigni] e Jagged1 hanno compiti importanti in altri organi e in altri tipi di cellule,” hanno spiegato il professor Adams e il dott. Benedito. “Questo rende difficile limitare gli effetti di [un farmaco] alle cellule dei vasi sanguigni. Speriamo comunque che il nostro lavoro porti allo sviluppo di nuove medicine.”
Per maggiori informazioni, visitare:
Cell:
http://www.cell.com
Società Max Planck:
http://www.mpg.de
Fonte: Società Max Planck; Cell
Documenti di Riferimento: Benedito, R. et al. (2009) The notch ligands Dll4 and Jagged1 have opposing effects on angiogenesis. Cell 137: 1124-35. DOI: 10.1016/j.cell.2009.03.025.