Distrofia Muscolare: dalla CRISPR una confortevole promessa
Sfruttando la capacità della tecnica di editing genetico CRISPR-Cas9 di tagliare ed eliminare con estrema precisione frammenti di DNA, tre studi indipendenti sul modello animale hanno mostrato che è possibile eliminare dal gene della distrofina, la proteina carente nella distrofia di Duchenne, la parte mutata che ne impedisce la sintesi.  Le cellule riprendono così a produrre una proteina che, per quanto non perfetta, permette un recupero della funzionalità muscolare.
Le cellule riprendono così a produrre una proteina che, per quanto non perfetta, permette un recupero della funzionalità muscolare.
Applicando la tecnica di editing genetico CRISPR-Cas9, ben tre gruppi di ricerca indipendenti hanno mostrato nel modello animale che è possibile arginare il degrado muscolare che caratterizza la distrofia muscolare di Duchenne e ottenere almeno un parziale recupero della forza. Gli studi sono pubblicati su “Science”.
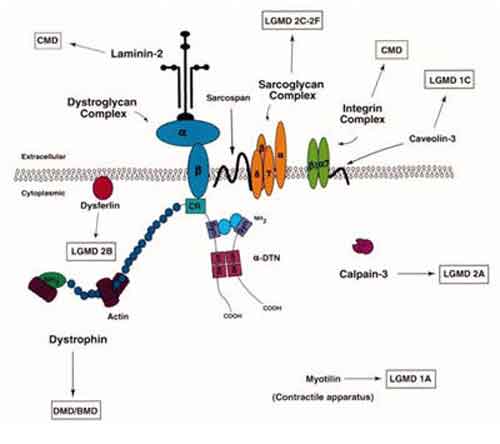
La distrofia muscolare di Duchenne è causata dall’incapacità del corpo di produrre distrofina, una lunga catena proteica che permette di legare una fibra muscolare alla struttura di supporto circostante. La distrofina è codificata da un gene contenente 79 regioni che concorrono alla codifica della proteina, chiamate esoni. Se uno di questi esoni è colpito da una mutazione nociva, la catena proteica non viene costruita. E senza la distrofina a tenere coese le fibre muscolari, il muscolo tende progressivamente a deteriorarsi fino a distruggersi.
Finora la terapia genica si era concentrata sul tentativo di introdurre nelle cellule una copia normale del gene non funzionante in modo che riacquistino la capacità di produrre la proteina mancante. Nonostante alcuni successi, tuttavia, questa tecnica deve affrontare il problema della corretta integrazione del nuovo gene, il cui inserimento nel punto sbagliato del genoma potrebbe a sua volta dimostrarsi nocivo.
Nel caso della distrofia di Duchenne, la CRISP-Cas9 segue un’altra strategia. Questa tecnica di editing genetico permette infatti di tagliare ed eliminare con estrema precisione un frammento di DNA: applicandola, i ricercatori hanno eliminato un esone mutante che bloccava il processo di trascrizione del gene e quindi la sintesi della distrofina. (Tutti e tre i gruppi hanno preso come bersaglio da eliminare l’esone 23 del gene della distrofina, che appare mutato nell’83 per cento dei pazienti affetti da distrofia di Duchenne.)
In questo modo il processo di trascrizione è in grado di arrivare a temine e portare a compimento la sintesi di una proteina di distrofina che, sia pure non perfetta, ha dimostrato di permettere un recupero della funzionalità muscolare nei topi affetti dalla forma murina della distrofia muscolare di Duchenne.
Per trasportare fino alle cellule muscolari di topi adulti il complesso CRISPR-Cas9, Charles A. Gersbach, della Duke University, e colleghihanno sfruttato il virus AAV8 (adenovirus-associato 8). Chengzu Long, dell’Università del Texas a Dallas, e colleghi hanno invece fatto ricorso, come vettore della CRISPR-Cas9, al virus AAV9, che ha un’affinità ancora superiore per le cellule muscolari, e così pure ha fatto il gruppo diretto daMohammadsharif Tabebordbar, della Harvard University.
“C’è ancora una notevole quantità di lavoro da fare per tradurre questi risultati in una terapia umana e dimostrarne la sicurezza”, ha detto Gersbach. “Ma l’esito dei nostri primi esperimenti è molto interessante. Ora punteremo all’ottimizzazione delle modalità di consegna del sistema di editing genetico, valutando l’efficacia dell’approccio in modelli della malattia più gravi, e la sua sicurezza in animali di maggiori dimensioni, con l’obiettivo finale di arrivare a test clinici.”