Tumore al colon: completato il reclutamento dei pazienti per lo studio PETACC-8 che valuta il Cetuximab
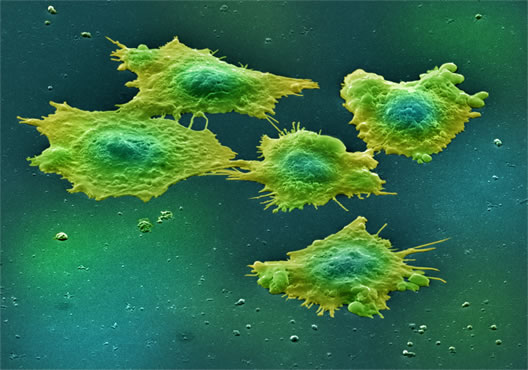
cellule tumore colon
Completato il reclutamento dei pazienti per lo studio PETACC-8 che valuta Cetuximab come trattamento adiuvante nel tumore al colon
• Si tratta del maggiore studio clinico paneuropeo volto a valutare il possibile ruolo di Cetuximab nel setting adiuvante per i pazienti colpiti da tumore del colon in stadio III con KRAS non mutato
• I l meccanismo di azione di Cetuximab indirizzato alle cellule è altamente efficace nella riduzione della massa tumorale e rappresenta una speranza per il successo dello studio
Darmstadt (Germania), 9 dicembre 2009 –Merck Serono, una divisione di Merck KGaA (Darmstadt, Germania), ha recentemente annunciato che è stato completato il reclutamento per lo studio clinico di Fase III, PETACC-8,a destinato a valutare l’efficacia di Cetuximab come trattamento del tumore al colon in stadio III nel setting adiuvante. PETACC-8 è uno studio clinico multinazionale, randomizzato, controllato, che è stato promosso e coordinato dalla Fédération Francophone de Cancérologie Digestive (FFCD) di Parigi. Lo studio ha reclutato con successo in tutta Europa i 2.566 pazienti necessari, con arruolamento iniziato nel 2005.
Lo studio clinico PETACC-8 valuta l’efficacia di Cetuximab a 6 mesi in associazione con la chemioterapia standard dopo l’asportazione chirurgica del tumore primario (il setting adiuvante) rispetto al trattamento col solo FOLFOX-4 in pazienti colpiti da tumore del colon allo stadio III; i pazienti presentavano un tumore KRAS non mutato e sono stati sottoposti a resezione totale del tumore (asportazione chirurgica). L’endpoint dello studio PETACC-8 è la sopravvivenza libera da malattia (DFS, Disease-Free Survival).i
“Purtroppo, in circa un terzo dei pazienti colpiti da tumore del colon allo stadio III, ai quali il tumore è stato completamente asportato chirurgicamente, il tumore si ripresenta. Trovare i modi per prevenire questa recidiva rappresenta quindi una priorità”, ha dichiarato il Dr. Julien Taïeb del Groupe Hospitalier Pitié-Salpêtrière, Parigi e sperimentatore principale dello studio PETACC-8, “Considerando soprattutto la costante efficacia dimostrata da Cetuximab nei pazienti con tumore metastatico del colon retto con KRAS non mutato siamo fiduciosi che questo studio raggiungerà il proprio endpoint primario.”
In adiuvante, l’obiettivo principale del trattamento è distruggere tutte le cellule tumorali che possano essere rimaste dopo che il tumore è stato asportato chirurgicamente. Si ipotizza che Cetuximab, essendo direttamente indirizzato a colpire le cellule tumorali attraverso il recettore del fattore di crescita epidermico (EGFR, Epidermal Growth Factor Receptor), sarà altamente efficace in questo setting.
“Attraverso lo studio PETACC-8, ci aspettiamo di ampliare il numero di risultati significativi recentemente osservati con Cetuximab nel tumore metastatico del colon retto” ha commentato il Dr. Olivier Kisker, Senior Vice-President, Global Clinical Development Unit Oncology, Merck Serono. “Nel tumore metastatico del colon retto, l’introduzione del test standard sullo stato del KRAS ha portato Cetuximab ad una posizione preminente nella cura personalizzata del tumore e ha dimostrato un aumento significativo dell’efficacia del trattamento in quei pazienti colpiti da tumori KRAS non mutato. Il successo dell’approccio personalizzato nella terapia del tumore metastatico del colon retto garantisce una speranza di cura nel setting adiuvante di questa patologia”.
Il tumore del colon retto è il terzo tipo di tumore più comune al mondo in termini di nuovi casi.ii Solo in Europa, ogni anno più di 413.000 persone sviluppano un tumore del colon retto, pari al 13% dell’incidenza totale dei tumori, 200.000 dei quali circa hanno un esito fatale.iii Ogni anno, in circa un quarto dei pazienti colpiti da tumore del colon retto che si presentano alla diagnosi, il tumore si è già diffuso oltre le pareti dell’intestino e ai linfonodi locali.iv Sebbene la chirurgia associata alla chemioterapia abbia portato ad un aumento significativo della sopravvivenza, circa un quarto dei pazienti probabilmente sarà colpito da una recidiva della patologia entro i tre anni.v Per questo motivo, è essenziale che siano valutate nuove terapie per diminuire il livello delle recidive e aumentare il tasso di sopravvivenza.
a PETACC-8: Pan-European Trial in Alimentary traCt Cancer #8
La FFCD
La FFCD è un’associazione no-profit, che ha sede in Francia, impegnata nell’ideazione, nella realizzazione, nelle analisi e nella pubblicazione di vasti studi clinici nell’oncologia dell’apparato digerente.
Per maggiori informazioni, visitare www.ffcd.fr
Bibliografia
i Clinicaltrials.gov. http://www.clinicaltrials.gov/ct2/show/NCT00265811.
ii Parkin DM, et al. Int J Cancer 2001;94(2):153-6.
iii Ferlay J, et al. Ann Oncol 2007;18:581-92.
iv NHS Center for Reviews and Dissemination, University of York, UK. Effective Health Care 1997;3(6). ISSN: 0965-0288.
v Andre T, et al. N Engl J Med 2004;350:2343-51.
Informazioni su Cetuximab
Cetuximab è un anticorpo monoclonale IgG1 di prima classe e ad ampia azione, indirizzato all’EGFR, il recettore del fattore di crescita epidermico. Come anticorpo monoclonale, la modalità di azione di Cetuximab si distingue dai trattamenti chemioterapici standard non selettivi in quanto punta in modo specifico e si lega all’EGFR. Il legame inibisce l’attivazione del recettore ed il successivo processo del segnale di traduzione, che comporta la riduzione sia dell’invasione dei tessuti sani da parte delle cellule tumorali sia l’espansione del tumore a nuovi siti. Si ritiene inoltre che inibisca l’attività sia delle cellule tumorali di riparare al danno causato dalla chemio e radioterapia e di inibire la formazione di nuovi vasi sanguigni all’interno dei tumori, che si traduce nel portare ad una globale soppressione della crescita tumorale.
L’effetto collaterale più comune con Cetuximab è uno sfogo epidermico simile all’acne che sembra essere correlato ad una buona risposta alla terapia. In circa 5% dei pazienti, reazioni di ipersensibilità possono comparire durante il trattamento con Cetuximab: circa la metà di queste reazioni è severa.
Cetuximab ha già ottenuto l’autorizzazione alla commercializzazione in 77 Paesi. E’ stato approvato per il trattamento del tumore del colon-retto metastatico in 77 Paesi e per il trattamento del tumore della testa e del collo a cellule squamose (SCCHN) in 72 Paesi:
• Dicembre 2003 (Svizzera), febbraio 2004 (Stati Uniti d’America), giugno 2004 (Unione Europea) e in seguito dagli altri Paesi: per l’uso in associazione con l’irinotecan nei pazienti con un tumore metastatico del colon retto (mCRC, metastatic colorectal cancer) esprimenti l’EGFR che hanno fallito la terapia con irinotecan. Inoltre, Cetuximab è stato anche approvato come agente singolo in altri pesi.
• Aprile 2006 (Unione Europea) e in seguito altri Paesi: per l’uso in associazione con la radioterapia per il trattamento del tumore localmente avanzato della testa e del collo a cellule squamose (SCCHN). In altri paesi, Cetuximab è anche approvato come monoterapia nei pazienti con un tumore SCCHN ricorrente e/o metastatico che hanno fallito la terapia con chemioterapia.
• Luglio 2008 (Unione Europea): l’autorizzazione è stata aggiornata per il trattamento dei pazienti che esprimono il recettore del fattore di crescita epidermico (EGFR), nel tumore mCRC con KRAS non mutato e come agente singolo nei pazienti che hanno fallito la terapia basata su oxaliplatino e irinotecan e che sono intolleranti all’irinotecan.
• Luglio 2008 (Giappone): per l’uso in associazione con irinotecan nei pazienti con tumore mCRC che esprime l’EGFR e che hanno fallito la precedente terapia con irinotecan
• Novembre 2008 (Unione Europea): l’autorizzazione è stata ampliata all’uso in associazione con la chemioterapia a base di platino nei pazienti colpiti da SCCHN ricorrente e/o metastatico.
Merck ha acquisito il diritto alla commercializzazione di Cetuximab fuori dagli Stati Uniti e dal Canada da ImClone Systems, una filiale totalmente di proprietà della Eli Lilly and Company, dal 1998. In Giappone, ImClone Systems Incorporated, Bristol-Myers Squibb Company e Merck sviluppano e commercializzano congiuntamente Cetuximab. Merck è attivamente impegnata nel progresso dei trattamenti in oncologia e sta studiando nuove terapie in aree specialistiche, quali l’uso di Cetuximab nel tumore del colon retto, della testa e del collo a cellule squamose e al polmone non a piccole cellule. Merck ha inoltre acquisito i diritti su un farmaco a base di tegafur-uracile – un chemioterapico orale somministrato con acido folinico (FA) per il trattamento di prima linea del tumore al colon-retto metastatico.
In campo oncologico, inoltre, Merck sta studiando l’uso del vaccino BLP25 liposoma nel trattamento del tumore al polmone non a piccole cellule. Il vaccino ha ottenuto lo status fast track nel Settembre 2004 da parte dell’FDA. Merck ha ottenuto una licenza esclusiva a livello mondiale da Oncothyreon Inc., Seattle, Washington, USA.
Inoltre, Merck sta sviluppando la cilengitide, che è la prima di una nuova classe di terapie anti-tumore investigazionali chiamate inibitori di integrina a raggiungere la fase III di svilupo; la cilegintide è attualmente studiata per il trattamento del glioblastoma, dell SCCHN e del NSCLC. Gli inibitori di integrina sono studiati per colpire il tumore e la sua vascolarizzazione.
Informazioni su Merck Serono
Merck Serono è la divisione per farmaci da prescrizione innovativi di Merck, gruppo globale farmaceutico e chimico. Merck Serono, con sede centrale a Ginevra, Svizzera, scopre, sviluppa, produce e commercializza piccole molecole innovative e farmaci biologici per aiutare pazienti affetti da patologie che non hanno ancora una risposta adeguata. Negli Stati Uniti e in Canada, EMD Serono opera separatamente attraverso affiliate incorporate.
Merck Serono offre prodotti all’avanguardia in oncologia, sclerosi multipla, infertilità, disfunzioni endocrine e del metabolismo. Non tutti i prodotti sono disponibili in tutti i mercati.
Con un investimento annuale in Ricerca & Sviluppo di circa 1 miliardo di euro, Merck Serono è impegnata a far crescere il proprio business sia in aree terapeutiche specialistiche come patologie neurodegenerative, Oncologia, Fertilità ed Endocrinologia, sia in nuove aree terapeutiche, a seguito dell’attività di ricerca sulle malattie autoimmuni ed infiammatorie.
Per maggiori informazioni, consultare il sito www.merckserono.it
Informazioni su Merck
Merck è un gruppo globale farmaceutico e chimico con vendite per 7,6 miliardi di Euro nel 2008, una storia iniziata nel 1668 ed un futuro formato da circa 33,000 dipendenti in 60 Paesi. Il suo successo è caratterizzato dall’innovazione da parte di dipendenti imprenditori. Le attività operative di Merck sono svolte sotto il coordinamento della Merck KgaA, nella quale la famiglia Merck detiene una partecipazione del 70% ed altri azionisti il rimanente 30%. Nel 1917 la succursale negli Stati Uniti Merck & Co è stata espropriata ed è divenuta da allora in poi una società indipendente.