TEVA annuncia i progressi degli studi sui farmaci biologici sperimentali valutati per il trattamento della neutropenia in pazienti con carcinoma mammario sottoposti a chemioterapia

– I risultati clinici per Lipegfilgrastim e Balugrastim sono stati presentati all’Oncology Conference; Teva è impegnata a proseguire i suoi programmi di sviluppo di farmaci biologici in Oncologia –
Gerusalemme, 12 luglio — Teva Pharmaceutical Industries Ltd. (NYSE: TEVA) ha annunciato la presentazione dei risultati clinici per i suoi farmaci biologici oncologici, Lipegfilgrastim e Balugrastim, avvenuta durante il simposio internazionale sulla terapia di supporto nel cancro della Multinational Association of Supportive Care in Cancer (MASCC) / International Society of Oral Oncology (ISOO), che si è tenuto a New York il 28 e 30 giugno scorsi.
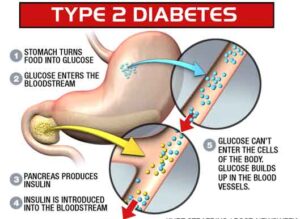
Lipegfilgrastim e Balugrastim sono fattori stimolanti le colonie granulocitarie (G-CSF) a lunga durata d’azione, studiati per la loro capacità di ridurre la durata della neutropenia severa in pazienti con carcinoma mammario sottoposti a chemioterapia. La neutropenia è la diminuzione del numero dei globuli bianchi nel sangue, che rende i pazienti più suscettibili a infezioni batteriche potenzialmente pericolose per la loro vita.
Entrambi i prodotti analizzati hanno completato gli studi di sperimentazione di fase III. In entrambi gli studi di fase III, condotti sul cancro al seno, è stato raggiunto l’endpoint primario, ovvero la riduzione della durata della neutropenia severa (DSN) al ciclo 1, paragonabile ai risultati ottenuti con pegfilgrastim, sia sotto il profilo dell’efficacia che della sicurezza. Al simposio MASCC / ISOO sono stati presentati, con presentazioni orali e con poster, anche ulteriori dati degli studi clinici di fase I, II e III di questi prodotti.
“Teva è impegnata a portare avanti lo sviluppo di questi farmaci biologici sperimentali, che sono i più avanzati tra i numerosi prodotti biologici che stiamo sviluppando”, ha detto il Dott. Michael Hayden, presidente Global R & D e Chief Scientific Officer di Teva Pharmaceutical Industries Ltd. “I farmaci biologici, finalizzati a offrire approcci sicuri ed efficaci ai pazienti con poche opzioni terapeutiche, costituiscono uno dei segmenti del mercato farmaceutico mondiale in più rapida crescita”.
G-CSF
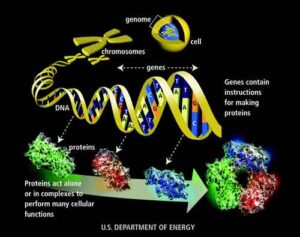
Il fattore di stimolazione delle colonie dei granulociti (G-CSF) è un ormone naturalmente prodotto dall’organismo, che stimola il midollo osseo a produrre neutrofili, un tipo di globuli bianchi che aiuta il sistema immunitario a combattere le infezioni. La chemioterapia può danneggiare la capacità dell’organismo di produrre neutrofili, causando neutropenia, cioè un basso numero di neutrofili nel sangue. La neutropenia è un effetto collaterale comune della chemioterapia ed espone i pazienti al rischio di infezione e sepsi. Una forma ricombinante di G-CSF (ovvero un farmaco biologico) viene usata per trattare pazienti affetti da tumore con neutropenia, per stimolare il midollo osseo a produrre più globuli bianchi.
Lipegfilgrastim e Balugrastim
Lipegfilgrastim è una forma glicosilata, peghilata, ricombinante di G-CSF. La peghilazione estende l’emivita del farmaco, permettendo una somministrazione meno frequente rispetto al G-CSF non peghilato. Balugrastim è un G-CSF ricombinante fuso con albumina umana. Sia Lipegfilgrastim sia Balugrastim sono stati concepiti per stimolare il midollo osseo a produrre globuli bianchi, in modo da ridurre la durata della neutropenia severa. La differenza fra le due molecole è costituita dai diversi meccanismi che utilizzano per raggiungere una emivita più lunga nel sangue.
TEVA
Teva Pharmaceutical Industries Ltd, è tra le prime aziende al mondo nel settore farmaceutico, da sempre impegnata nel rendere accessibili terapie di cura di alta qualità attraverso lo sviluppo, la produzione e la commercializzazione sia di farmaci equivalenti che di farmaci innovativi, specialità farmaceutiche e principi attivi. Con sede centrale in Israele, Teva è la leader mondiale nel mercato dei farmaci equivalenti, con un portfolio prodotti globale di oltre 1300 molecole e una presenza diretta in circa 60 Paesi. Le aree terapeutiche su cui Teva concentra le sue attività brand sono il SNC, l’oncologia, il dolore, l’apparato respiratorio, la salute della donna così come le biotecnologie.
Teva oggi conta 46000 dipendenti nel mondo e nel 2011 ha registrato un fatturato mondiale di 18,3 miliardi di dollari.
Teva’s Safe Harbor Statement under the U. S. Private Securities Litigation Reform Act of 1995:
This release contains forward-looking statements, which express the current beliefs and expectations of management. Such statements are based on management’s current beliefs and expectations and involve a number of known and unknown risks and uncertainties that could cause our future results, performance or achievements to differ significantly from the results, performance or achievements expressed or implied by such forward-looking statements, including statements relating to the results of the GALA phase III trial and the potential efficacy or future market or marketability of glatiramer acetate 40 mg/1 ml. Following further analysis, Teva’s interpretation of the results could differ materially depending on a number of factors, and we caution investors not to place undue reliance on the forward-looking statements contained in this press release as there can be no guarantee that the results from the phase III trial discussed in this press release will be confirmed upon full analysis of the results of the trial and additional information relating to the safety, efficacy or tolerability of glatiramer acetate 40 mg/1 ml may be discovered upon further analysis of data from the phase III trial. Even if the results described in this release are confirmed upon full analysis of the GALA study, we cannot guarantee that glatiramer acetate 40 mg/1 ml will be approved for marketing in a timely manner, if at all, by regulatory authorities in the EU or in the U.S. Important factors that could cause or contribute to such differences include risks relating to: our ability to develop and commercialize additional pharmaceutical products, competition for our innovative products, especially Copaxone® (including competition from innovative orally-administered alternatives, as well as from potential generic equivalents), competition for our generic products (including from other pharmaceutical companies and as a result of increased governmental pricing pressures), competition for our specialty pharmaceutical businesses, our ability to achieve expected results through our innovative R&D efforts, the effectiveness of our patents and other protections for innovative products, decreasing opportunities to obtain U.S. market exclusivity for significant new generic products, our ability to identify, consummate and successfully integrate acquisitions (including the acquisition of Cephalon), the effects of increased leverage as a result of the acquisition of Cephalon, the extent to which any manufacturing or quality control problems damage our reputation for high quality production and require costly remediation, our potential exposure to product liability claims to the extent not covered by insurance, increased government scrutiny in both the U.S. and Europe of our agreements with brand companies, potential liability for sales of generic products prior to a final resolution of outstanding patent litigation, including that relating to the generic version of Protonix®, our exposure to currency fluctuations and restrictions as well as credit risks, the effects of reforms in healthcare regulation and pharmaceutical pricing and reimbursement, any failures to comply with complex Medicare and Medicaid reporting and payment obligations, governmental investigations into sales and marketing practices (particularly for our specialty pharmaceutical products), uncertainties surrounding the legislative and regulatory pathway for the registration and approval of biotechnology-based products, adverse effects of political or economical instability, major hostilities or acts of terrorism on our significant worldwide operations, interruptions in our supply chain or problems with our information technology systems that adversely affect our complex manufacturing processes, any failure to retain key personnel (including Cephalon employees) or to attract additional executive and managerial talent, the impact of continuing consolidation of our distributors and customers, variations in patent laws that may adversely affect our ability to manufacture our products in the most efficient manner, potentially significant impairments of intangible assets and goodwill, potential increases in tax liabilities, the termination or expiration of governmental programs or tax benefits, environmental risks and other factors that are discussed in our Annual Report on Form 20-F for the year ended December 31, 2011 and in our other filings with the U.S. Securities and Exchange Commission. Forward-looking statements speak only as of the date on which they are made and the Company undertakes no obligation to update or revise any forward-looking statement, whether as a result of new information, future events or otherwise.