Il silenziamento di uno dei due cromosomi X
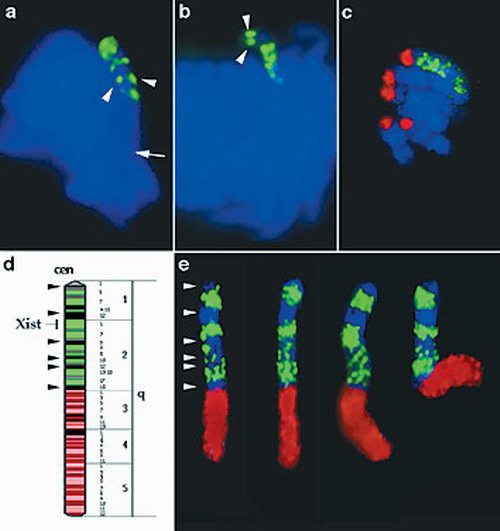
Localizzazione dell'XIST RNA, durante la metafase, in una cellula murina
Nelle prime fasi del loro sviluppo, le cellule di mammifero femmina reagiscono alla presenza di un doppio cromosoma X rivestendo uno di essi con un lungo filamento di RNA chiamato XIST. L’RNA si lega allo stesso cromosoma X da cui è trascritto e innesca una serie di eventi che portano al silenziamento permanente del cromosoma.
La scoperta di questo processo risale a oltre dieci anni fa, ma finora ben poco si sapeva sui meccanismi con cui questo RNA non codificante lungo 14 chilobasi si legasse al suo bersaglio. Ora, come viene illustrato in un articolo sul “Journal of Cell Biology” un gruppo di ricercatori della University of Massachusetts Medical School ha mostrato che XIST si dissocia temporaneamente del cromosoma X inattivato (Xi) durante la mitosi e che la proteina Aurora B chinasi concorre a regolarne il legame alla cromatina. “Sappiamo che esso non si lega semplicemente al DNA, ma non sono state finora identificate specifiche proteine di legame”, spiega Lisa Hall, che con Jeanne Lawrence ha diretto lo studio.
Gli usuali approcci biochimici per identificare le proteine di legame sono stati ostacolati dalle notevoli dimensioni di XIST e dalla sua forte adesione al cromosoma X, che ne rendono molto difficile l’estrazione e lo studio in vitro. Per questo Hall e colleghi hanno deciso di optare per un approccio in vivo, riproducendo gli eventi che provocano l’allontanamento di XIST dall’Xi all’inizio della profase del ciclo cellulare.
I ricercatori hanno in particolare scoperto che trattando le cellule con un inibitore della proteina fosfatasi 1 (PP1) si provoca il rilascio di XIST dall’Xi nelle cellule che si trovano nell’interfase. PP1 normalmente tiene sotto controllo Aurora B fino all’inizio della mitosi, ma l’aumento di attività della Aurora B ha determinato il precoce rilascio di XIST. XIST non veniva invece più rilasciato durante l’interfase se venivano inibiti sia PP1 sia Aurora B. Infine, l’inibizione di Aurora B faceva sì che XIST restasse ancorato a Xi anche nelle cellule in mitosi.
Studi precedenti dello stesso gruppo di ricerca avevano suggerito che il legame di XIST potesse essere controllato da un principio organizzatore della cromatina, e che esso avesse un ruolo anche nelle cellule cancerose, quando la regolazione di XIST e di Xi spesso fallisce. Aurora B, osservano i ricercatori, corrisponde bene a questo profilo, in quanto si localizza sui bracci del cromosoma durante la profase, fosforila diverse proteine della cromatina, fra cui l’istone H3, e risulta spesso attivata nelle cellule cancerose.
XIST può rappresentare un’ampia classe di RNA non codificanti che sono associati e regolano l’eterocromatina. “Speriamo che la manipolazione del legame in vivo rappresenti un nuovo modo di studiare le interazioni RNA-cromatina e che venga utilizzato anche da altri laboratori”, ha detto la Lawrence. “Sarà interessante stabilire se anche altri RNA rispecchiano il comportamento di XIST e sono controllati dallo stesso meccanismo.”